- RÉSONANCE (chimie)
- RÉSONANCE (chimie)Étymologiquement, le mot «résonance» s’applique au renforcement de l’intensité vibratoire ou sonore. Il évoque donc essentiellement un phénomène mécanique. Heisenberg, en 1926, l’utilisa pour la première fois en mécanique quantique dans ses travaux sur les systèmes d’oscillateurs couplés. C’est Pauling, dans ses recherches sur la nature de la liaison chimique, vers 1930, qui l’introduisit en chimie, lui donnant un sens tout différent. Dans l’impossibilité d’attribuer à certaines molécules, le benzène par exemple, une formule unique, on est conduit à envisager la structure réelle comme intermédiaire entre plusieurs formes, dites limites. Bien que sa structure soit unique, on dit que la molécule est dans un état de résonance, ou plus simplement, résonne, entre les diverses formes limites envisagées. Cette situation entraîne des différences notables entre les propriétés physico-chimiques de la molécule réelle et celles que posséderaient les formes limites fictives.Pour bien saisir le concept de la résonance dans les molécules, il est indispensable de préciser son sens exact en mécanique quantique. En mécanique classique, la résonance n’est en fait qu’un aspect très particulier du couplage entre systèmes vibratoires, qui se manifeste pour certaines valeurs des paramètres définissant ces systèmes par une augmentation très importante de l’intensité vibratoire [cf. VIBRATIONS MÉCANIQUES]. Si, dans la théorie des systèmes vibratoires, en mécanique quantique, le couplage se manifeste aussi, la résonance, au sens classique, n’apparaît pas. On sait en effet qu’en mécanique quantique on ne peut connaître simultanément la position et la vitesse d’une particule mais seulement déterminer la probabilité de trouver à un instant t une particule en un point donné, probabilité qui est prise égale au carré du module de la fonction d’onde (cf. mécanique QUANTIQUE). Dans le cas particulier d’un système isolé, l’énergie est constante et la probabilité en question ne dépend plus du temps, mais seulement du point considéré. On dit que le système est dans un état stationnaire.DéfinitionLe problème de la détermination de la structure d’une molécule et de ses propriétés se ramène à la résolution de l’équation de Schrödinger correspondante. Mais cette équation différentielle du second ordre n’est pas intégrable dans le cas général, et des solutions approchées doivent être recherchées. Parmi les méthodes utilisées, le calcul des variations constitue un procédé de choix. Il consiste à chercher pour solution approchée de l’équation de Schrödinger une combinaison linéaire de fonctions d’onde que l’on se donne a priori et auxquelles on demande de former une base de développement acceptable. Dans le cas particulier des molécules, on peut choisir pour base des fonctions d’onde décrivant les diverses paires d’électrons localisées, selon les conceptions classiques, soit entre deux atomes, soit sur un atome. Dans le premier cas, la paire d’électrons est schématisée par un tiret entre les atomes; dans le second, ou bien on a une paire d’électrons libres, représentés par deux points, comme dans l’ammoniac: NH3, ou bien on a des ions.Par construction, la fonction d’onde est donc une combinaison linéaire des diverses fonctions de base introduites. Pour la molécule d’hydrogène, par exemple, on prendra pour base de développement les fonctions correspondant aux trois formes limites: H 漣H, H+H- et H-H+. Par analogie avec le cas des oscillateurs couplés (cf. OSCILLATEURS et VIBRATIONS MÉCANIQUES), Pauling a parlé de résonance entre les formes limites qui joueraient ainsi le rôle des oscillateurs indépendants primitifs. Symboliquement, on présente la structure réelle par le schéma conventionnel:
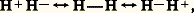 qui évoque une oscillation des charges électroniques d’une forme à l’autre. On notera l’utilisation de la flèche double qui ne doit pas être confondue avec les deux flèches orientées en sens inverse l’une par rapport à l’autre (face=F0019 燎) servant à indiquer un équilibre entre les constituants réellement présents dans un système chimique. Il est question ici d’une espèce chimique unique, intermédiaire, mésomère , entre les formes limites envisagées.L’analogie entre le phénomène classique d’oscillations couplées et la structure moléculaire est bien mince et l’emploi du même terme de résonance ne peut être que source de malentendus. Le mot a pourtant fait fortune, et son emploi est devenu classique.Quelques applicationsC’est surtout dans le domaine des molécules conjuguées que la notion de résonance a été appliquée. Le cas le plus typique est celui du benzène. Les trois doubles liaisons du schéma classique de Kékulé ne sont pas indépendantes mais ont fusionné en un système unique, totalement symétrique, le noyau benzénique [cf. AROMATICITÉ]. Sans atteindre ce degré d’importance, le phénomène subsiste dans des molécules comme le butadiène où les doubles liaisons sont encore reconnaissables. Cette réorganisation des électrons est aussi connue sous le nom de conjugaison des systèmes insaturés. Cette appellation est préférable au mot «résonance», car non seulement elle n’évoque pas d’image fausse, mais, étymologiquement, elle signifie bien que les systèmes primitifs ont fusionné en un seul.L’établissement de la conjugaison entre les diverses liaisons doubles ou triples d’une molécule, ou encore d’un système de liaisons multiples avec les électrons d’une paire libre portée par un atome voisin, se traduit par un certain nombre de modifications des propriétés physico-chimiques par rapport aux schémas de référence fictifs donnés par la graphie classique.Modification des longueurs des liaisonsPour le benzène, par exemple, toutes les liaisons chimiques sont égales (0,140 nm), ce qui correspond à un allongement des doubles liaisons, qui, isolées, mesureraient 0,133 nm, et à un raccourcissement des simples liaisons, qui, isolées, mesureraient 0,152 nm. Dans le butadiène, l’effet est moins marqué, mais la différenciation entre les liaisons terminales (0,134 nm) et la liaison centrale (0,147 nm) reste très nette.L’effet est surtout sensible lorsque le système conjugué possède un hétéroatome, comme dans l’acroléine. À partir de l’atome d’oxygène, plus électronégatif que les carbones, on observe une polarité alternée: C+ 漣C- 漣C+ 漣-. Le phénomène peut se manifester aussi avec des atomes de même nature, comme dans le fulvène (formule 1), ce qui entraîne l’apparition d’un moment dipolaire d’environ 1 debye.Modification des spectres d’absorptionEn général, la conjugaison se traduit par un déplacement de la première bande d’absorption électronique vers les grandes longueurs d’onde (effet bathochrome) et par un abaissement des fréquences de vibration des divers groupements de la molécule.Stabilisation énergétiqueToutefois, le phénomène majeur pour le chimiste est la stabilisation de la molécule conjuguée par rapport à la molécule fictive non conjuguée. L’effet peut être chiffré par l’abaissement d’énergie correspondant, appelé énergie de résonance ou de conjugaison. Parmi les applications les plus intéressantes, il y a lieu de mentionner le cas des systèmes en équilibre que la conjugaison va orienter dans un sens bien déterminé. Par exemple, lorsqu’on a deux isomères, comme dans le cas d’une cétone et de sa forme énolique (formule 2), la forme cétonique est plus stable que la forme énolique, d’où la prépondérance à peu près exclusive de la première dans les cétones non conjuguées.Si un système insaturé est greffé sur le carbone porteur de l’hydrogène, la forme énolique sera plus stabilisée que la forme cétonique. Dans le cas du phénol, la forme énolique pourra devenir prépondérante.Le cas des réactions où plusieurs isomères sont susceptibles de se former est semblable. Par le jeu des équilibres qui s’établissent, c’est l’isomère le plus conjugué, car le plus stable, qui sera prépondérant.Un autre exemple typique d’application est le renforcement de l’acidité des acides carboxyliques conjugués: ce phénomène est dû au fait que l’ion carboxylate R 漣C-2 est plus conjugué que l’acide lui-même R 漣C2H et, par conséquent, plus stabilisé quand le radical R est un groupement insaturé comme dans le cas de l’acide benzoïque C6H5 漣C2H.
qui évoque une oscillation des charges électroniques d’une forme à l’autre. On notera l’utilisation de la flèche double qui ne doit pas être confondue avec les deux flèches orientées en sens inverse l’une par rapport à l’autre (face=F0019 燎) servant à indiquer un équilibre entre les constituants réellement présents dans un système chimique. Il est question ici d’une espèce chimique unique, intermédiaire, mésomère , entre les formes limites envisagées.L’analogie entre le phénomène classique d’oscillations couplées et la structure moléculaire est bien mince et l’emploi du même terme de résonance ne peut être que source de malentendus. Le mot a pourtant fait fortune, et son emploi est devenu classique.Quelques applicationsC’est surtout dans le domaine des molécules conjuguées que la notion de résonance a été appliquée. Le cas le plus typique est celui du benzène. Les trois doubles liaisons du schéma classique de Kékulé ne sont pas indépendantes mais ont fusionné en un système unique, totalement symétrique, le noyau benzénique [cf. AROMATICITÉ]. Sans atteindre ce degré d’importance, le phénomène subsiste dans des molécules comme le butadiène où les doubles liaisons sont encore reconnaissables. Cette réorganisation des électrons est aussi connue sous le nom de conjugaison des systèmes insaturés. Cette appellation est préférable au mot «résonance», car non seulement elle n’évoque pas d’image fausse, mais, étymologiquement, elle signifie bien que les systèmes primitifs ont fusionné en un seul.L’établissement de la conjugaison entre les diverses liaisons doubles ou triples d’une molécule, ou encore d’un système de liaisons multiples avec les électrons d’une paire libre portée par un atome voisin, se traduit par un certain nombre de modifications des propriétés physico-chimiques par rapport aux schémas de référence fictifs donnés par la graphie classique.Modification des longueurs des liaisonsPour le benzène, par exemple, toutes les liaisons chimiques sont égales (0,140 nm), ce qui correspond à un allongement des doubles liaisons, qui, isolées, mesureraient 0,133 nm, et à un raccourcissement des simples liaisons, qui, isolées, mesureraient 0,152 nm. Dans le butadiène, l’effet est moins marqué, mais la différenciation entre les liaisons terminales (0,134 nm) et la liaison centrale (0,147 nm) reste très nette.L’effet est surtout sensible lorsque le système conjugué possède un hétéroatome, comme dans l’acroléine. À partir de l’atome d’oxygène, plus électronégatif que les carbones, on observe une polarité alternée: C+ 漣C- 漣C+ 漣-. Le phénomène peut se manifester aussi avec des atomes de même nature, comme dans le fulvène (formule 1), ce qui entraîne l’apparition d’un moment dipolaire d’environ 1 debye.Modification des spectres d’absorptionEn général, la conjugaison se traduit par un déplacement de la première bande d’absorption électronique vers les grandes longueurs d’onde (effet bathochrome) et par un abaissement des fréquences de vibration des divers groupements de la molécule.Stabilisation énergétiqueToutefois, le phénomène majeur pour le chimiste est la stabilisation de la molécule conjuguée par rapport à la molécule fictive non conjuguée. L’effet peut être chiffré par l’abaissement d’énergie correspondant, appelé énergie de résonance ou de conjugaison. Parmi les applications les plus intéressantes, il y a lieu de mentionner le cas des systèmes en équilibre que la conjugaison va orienter dans un sens bien déterminé. Par exemple, lorsqu’on a deux isomères, comme dans le cas d’une cétone et de sa forme énolique (formule 2), la forme cétonique est plus stable que la forme énolique, d’où la prépondérance à peu près exclusive de la première dans les cétones non conjuguées.Si un système insaturé est greffé sur le carbone porteur de l’hydrogène, la forme énolique sera plus stabilisée que la forme cétonique. Dans le cas du phénol, la forme énolique pourra devenir prépondérante.Le cas des réactions où plusieurs isomères sont susceptibles de se former est semblable. Par le jeu des équilibres qui s’établissent, c’est l’isomère le plus conjugué, car le plus stable, qui sera prépondérant.Un autre exemple typique d’application est le renforcement de l’acidité des acides carboxyliques conjugués: ce phénomène est dû au fait que l’ion carboxylate R 漣C-2 est plus conjugué que l’acide lui-même R 漣C2H et, par conséquent, plus stabilisé quand le radical R est un groupement insaturé comme dans le cas de l’acide benzoïque C6H5 漣C2H.
Encyclopédie Universelle. 2012.
